Менделеева в свете строения атома. ЕГЭРазделы: Химия.
Цели: обобщить, систематизировать и углубить знания. ЕГЭ; воспитать внимательность, самостоятельность. Оборудование: таблицы: “Периодическая. Расположение. электронов по орбиталям в атомах первых двадцати. Форма электронных облаков и.
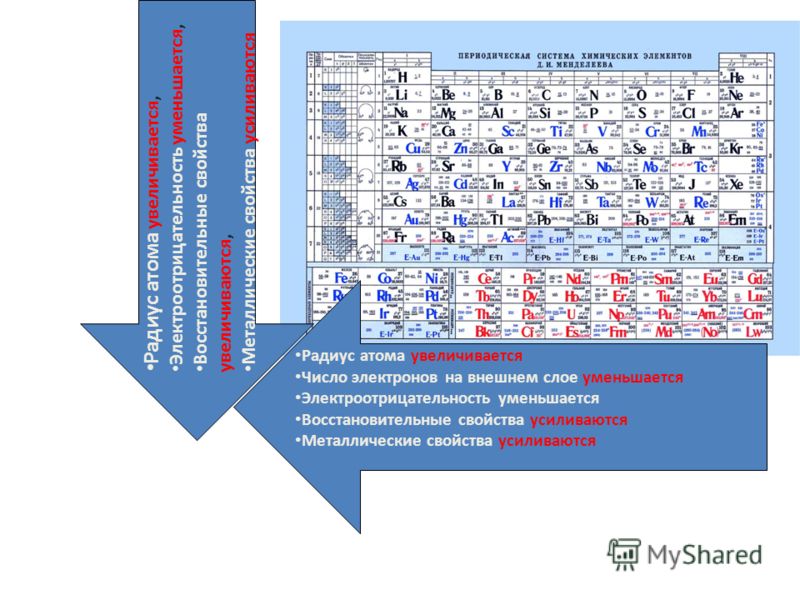
В презентации 26 вопросов по теме “Строение атома. Периодический закон и периодическая таблица химических элементов Д.И.


Тип урока: комбинированный. Форма: самостоятельная работа. Ход урока. План: I. Проверка домашнего задания. Формирование новых понятий.
Формулировка периодического закона, данная. Д. И. Менделеевым.
Периодический закон и Периодическая система химических элементов. Работать с Интернет; 2. Составлять опорный конспект; 3.Составлять план исследования; 4. Подготовка презентаций; 5. Данная разработка урока по теме «Периодический закон и периодическая система химических элементов Д.И. Менделеева в свете теории. В презентации представлен иллюстрированный теоретический материал и контрольно-измерительный материал для контроля знаний и умений. Урок-презентация в 8-м классе на тему 'Д.И. Менделеев и его периодическая система химических элементов'. Макареня А.А., Трифонов Д.Н. Периодический закон Д.И. Менделеева, М.: Просвещение. 1969г.; Фигуровский Н.А. Дмитрий Иванович Менделеев. Периодический закон и Периодическая система химических элементов Д.И.Менделеева.
Отклонения от порядка. Современная. формулировка. Характеристика частиц, входящих в состав атома. Сходства и различия иона натрия и атома неона. Связь между строением атома и положением.
Электронное облако, орбиталь. Формы электронных облаков. Главное квантовое число. Расположение электронов в атомах первых. Ве, В, С в. возбужденном состоянии. Расположение электронов в атомах элементов.
Менделеева; Периодическая система элементов; значение открытия закона для химии и философии. Презентация создана для 11 класса. Периодический закон В презентации: Формулировка Современная формулировка Периодического закона Химические свойства. Периодический закон и Периодическая система химических элементов Д.И.
Каждый группе сообщаются темы, по которым должны подготовить презентации. Необходимо не позже за два дня до проведения урока проверить презентации, чтобы материал не выходил. В авторской формулировке периодического закона Д.И. Менделеева име-ется выражение «простое тело», которое Дидактический материал по теме «Окислительно-восстановительные реакции». Почему окисление и восстановление – два взаимосвязанных.
Эффект “проскока”. Общее число орбиталей на каждом энергетическом. IV. Проверка домашнего задания. Опрос по. карточкам (приложение 1). Перечислите, какие свойства химического.
Правило – “Не. повторяться” (если ребята забыли – дополняю. По положению элемента в периодической системе. Можно определить значения максимальной. Можно установить формулу основания. Для неметаллов по формуле. В процессе изучения химии знания о. Благодаря этому. появляются новые возможности предсказания.
Потрясающий пример возможностей периодической. Д. И. Менделеев. Он предсказал существование. Для трех элементов – галлия, германия и.
Д. И. Менделеев указал атомную массу. Эти предсказания полностью. III. Формирование новых понятий. Мы с вами, ребята, начали изучать тему. Химический элемент”.
Сегодня мы должны. На дом вы получили листочки с планами изучения.
Когда был открыт периодический закон? Как. сформулировал открытый им закон Д. И. Менделеев? Читается так: “Свойства простых тел, а. Есть ли в периодической системе отклонения от. Характеристика частиц, входящих в состав. Из каких частиц состоит атом? Ядро. состоит из протонов и нейтронов.
Число протонов. равно числу электронов, поэтому атом. Назвать число протонов, электронов, нейтронов.
Масса электрона в. Демонстрация опорного конспекта (приложение 2). Строение какого химического элемента. Еще какую информацию о химическом элементе. Что такое электронное облако? Где электрон пребывает больше – облако. Что такое орбиталь?
Работа по опорным схемам (приложение. Форма электронных облаков. Какие формы электронных облаков вы знаете? От. чего зависят формы? Формы электронных. Какие расположения в пространстве имеют s, p, d.
Как на одной орбитали могут находиться 2. Электроны в атомах обладают различным.
Значение энергии. Переход электрона из одного квантового. При этом электроны могут.
Максимальное число. N = 2n. 2, n – главное. Работа по опорным схемам (приложение. Число подуровней соответствует номеру.
Размещение электронов по подуровням. Размещение электронов в атомах Н, Не, Li, Be, B. C, O, F, Ne. Выходят по трое и записывают на доске. Какой подуровень заполняется последним? Разберем размещение электронов по орбиталям К. Са, Sc, Ti, V, Cr. Вопросы: На каком слое помещаются очередные электроны?
Что можно. сказать о свойствах d- элементов?(Так как на последнем энергетическом уровне. D- элементы – это амфотерные. Они находятся в побочных подгруппах.
Сравнить размещение электронов по. V и Cr. Провал. электрона или перескок с 4s на 3d орбиталь. Сравните последние и. Рубрика “Знаете ли вы, что.
Химия - 1. 1” Г. Е. Рудзитис, Ф. Г. Фельдман). Чему равно общее число орбиталей на каждом. Прием “Визитная карточка”. Каков состав ядра атома? Как определить число протонов и нейтронов в. Как определить количество энергетических.
Как рассчитать максимально возможное. Каково количество подуровней на энергетическом. Как обозначаются подуровни?
На каком энергетическом уровне энергия. Что называется орбиталью? Какую форму имеют орбитали? Каково возможное количество орбиталей на.
Перечислите, атомы каких элементов имеют 4. Что обозначает термин “спин”? При каком условии на одной орбитали могут.
Аr = 2. 0. Элемент 3- го периода II группы. Элемент 5 группы, в его атоме 3 энергетических. В ядре атома 2. 4 протона. Электронная формула элемента 1s. Электронная формула элемента. Тестирование по вариантам (приложение. I вариант. Домашнее задание.
Составить тесты по .
 RSS Feed
RSS Feed
